

生物質(如木質纖維素)可轉化為重要的平臺分子呋喃類化合物(如羥甲基糠醛、糠醛)。但現(xiàn)有的后續(xù)轉化(生產(chǎn)琥珀酸、1,4-丁二醇等)均涉及氧化或還原過程,改變了分子本身的氧化還原水平,造成了能量和原子經(jīng)濟性的浪費(圖1)。從呋喃直接通過中性水解生成1,4-二羰基化合物(如琥珀醛),在熱力學上是吸能過程。傳統(tǒng)酸催化嘗試會引發(fā)嚴重的呋喃聚合副反應,因此被認為是不可行的。
本文報道了一種解決該問題的光化學方法,該方法通過1,6-二氧雜環(huán)癸烯中間體(圖1C)驅動呋喃水解反應,同時抑制聚合反應。由此得到的有價值的1,4-酮醛1i現(xiàn)在可以直接從呋喃獲得。此外,本文的策略還通過糠醛衍生物的水解和Nazarov環(huán)化反應,實現(xiàn)了反式二羥基環(huán)戊烯酮1j的合成。

圖1. 背景介紹及本文的工作(圖片來源:Science)
首先,作者認為可見光可以提供克服呋喃水解熱力學障礙所需的能量。選擇2-戊基呋喃(2d)作為優(yōu)化底物,并結合使用均三甲苯-吖啶光催化劑PCI和450 nm發(fā)光二極管(LED)照射(圖2A)。找到了最佳條件I [2.5 mol% PCI,450 nm LED,MeCN:H2O,2:1 (v:v),0.20 M],核磁共振(NMR)測得產(chǎn)物3d的產(chǎn)率為74%,其中包含了由于起始原料聚合造成的不可避免的損失。
使用條件I后,多種2-烷基取代呋喃(2a-2o)被水解為其相應的 γ-酮醛(3a- 3o,分離產(chǎn)率21%-79%;圖2A)。該催化體系對2-烷基取代基的變化表現(xiàn)出良好的兼容性。此外,連接的醚和硫醇(3g和3h)、硫酯(3i)、酯(3j和 3k)以及醛(3l)也與該體系兼容。3m之前是通過多步反應從呋喃2m合成的,包括氧化、還原,最后進行水解。而本文的方法只需一步即可從相同的起始原料2m直接獲得該產(chǎn)物,產(chǎn)率為 54%。
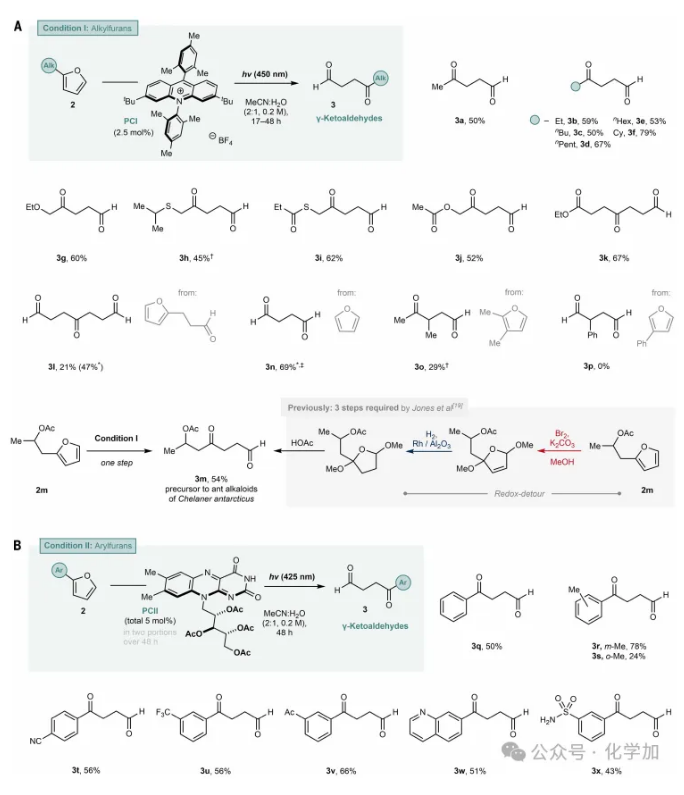
圖2. 呋喃水解的底物范圍(圖片來源:Science)
本文的方法實現(xiàn)了呋喃(2n)水解生成琥珀醛(3n),產(chǎn)率為69%(通過1H NMR 測定)。該方法的局限性體現(xiàn)在3-烷基取代呋喃上,只有呋喃2o轉化為產(chǎn)物3o,產(chǎn)率為23%,而其他底物則沒有反應性(2p)。這與Park等人觀察到的反應性形成鮮明對比,他們發(fā)現(xiàn)3-取代呋喃是轉化為吡咯的最成功的底物。這暗示著不同的反應機理。
2-芳基取代的呋喃底物在條件I下沒有發(fā)生轉化。經(jīng)過全面的篩選實驗,確定了最佳反應條件II,該條件使用(?)-核黃素四乙酸酯PCII作為光催化劑,并使用425 nm光源(圖2B)。這類底物的反應速度較慢,需要2天的反應時間,并且需要分兩次加入催化劑,這可能是由于光催化劑的漂白效應所致。在條件II下,電中性底物(2q-2s),以及缺電子底物(2t-2x),均獲得了令人滿意的產(chǎn)率(43%-78%)。總的來說,反應動力學對取代模式及其對芳基的電子效應非常敏感。如,2-(間甲苯基)呋喃以78%的產(chǎn)率得到產(chǎn)物3r,但2-(鄰甲苯基)呋喃2s的轉化率卻很低。

圖3. 機理研究(圖片來源:Science)
通過在線LED-NMR、EPR、同位素標記實驗與理論計算的緊密結合,作者排除了傳統(tǒng)猜想(如通過烯醛中間體的光氧化還原循環(huán)),并詳細闡明了反應歷程:啟動:呋喃被光催化劑氧化為自由基陽離子 I。二聚: I 進攻另一分子中性呋喃,形成二聚自由基陽離子 II。重排與開環(huán): 經(jīng)過逐步的dyotropic型重排和擴環(huán),形成關鍵的1,6-二氧雜環(huán)癸烯中間體 A(其結構通過NMR和計算確認)。水解: 中間體 A 最終水解生成琥珀醛。該機理與已知的3-取代呋喃轉化途徑不同,解釋了本方法對2-取代呋喃的選擇性(圖3)。

圖4. 糠醛衍生物的光水解反應(圖片來源:Science)
接下來,將注意力轉向糠醛衍生物。使用糠醛5a和Fukuzumi原位形成的吖啶-Sc(OTf)3催化劑復合物(條件III-A),在425 nm光照射下,得到的不是開環(huán)產(chǎn)物,而是反式二羥基環(huán)戊烯酮6a,產(chǎn)率為81%。反式二羥基結構已通過固態(tài)結構分析證實(圖4A)。這種轉化可以被概念化為一種氧化還原中性反應類型,比Piancatelli反應高一個氧化還原水平,該反應從糠醇衍生物出發(fā)生成單羥基環(huán)戊烯酮(圖4B)。
糠醛衍生物5b和5c在條件III-A下也能發(fā)生轉化(圖4C)。對于烷基呋喃酮5d和5e,Al(OTf)3作為路易斯酸表現(xiàn)更佳(條件III-B)。這些條件也使得從市售的甲基呋喃酮5d出發(fā),兩步即可合成抗生素(±)-epi-Pentenomycin I(69%)和(±)-epi-Pentenomycin III(36%)。此前,這些目標化合物的合成需要七步以上。
一旦呋喃環(huán)上引入更多取代基,反應活性就會急劇下降。Ritter的吖啶衍生物3,6-二甲基-9-(2,4,6-三氯苯基)吖啶(條件III-C)可以恢復底物5f和天然產(chǎn)物艾蒿酮(5g)的反應活性,在對催化劑用量和比例進行微調(diào)后,分別得到產(chǎn)物6f(產(chǎn)率64%)和6g(產(chǎn)率43%)。羥甲基糠醛(5h)也表現(xiàn)出反應活性,但由于其在反應過程中分解,最終產(chǎn)物6h的產(chǎn)率僅為17%。
此前,獲得反式二羥基環(huán)戊烯酮結構一直比較困難,如(±)-Terrein的合成就十分艱難或產(chǎn)率很低。相比之下,能夠通過Suzuki偶聯(lián)反應將丙烯基側鏈引入生成的溴化物6b,以市售呋喃5b為原料,通過一鍋兩步法合成(±)-Terrein,產(chǎn)率高達47%(圖4C)。
此外,還通過保護基策略,以6i和6j為中間體,從頭合成天然產(chǎn)物(±)-Trichoderone。這些合成實例表明,本文的氧化還原中性光水解方法可以巧妙地獲得五烯霉素、木霉素或濕傘酮家族中常見的難以獲得的順式二羥基環(huán)戊烯酮結構,這些結構對于藥物抗菌研究具有重要意義。
為了理解這種糠醛水解反應的潛在機理,再次使用光纖耦合的450 nm LED 1H NMR對反應進行了跟蹤。提出了一種類似于Piancatelli反應的途徑(圖4D),其中初始的光催化氧化是限速步驟。最終的立體選擇性熱協(xié)同旋轉4π-電環(huán)化反應決定了最終產(chǎn)物中反式二羥基官能團的構型,而光Nazarov型環(huán)化反應似乎并未發(fā)生。盡管如此,對照實驗表明,該反應僅在光照條件下才能發(fā)生,從而實現(xiàn)了糠醛的上坡轉化(ΔG = +7.2 kcal mol?1),這使其與已知的Piancatelli反應(甲基糠醇的ΔG = ?7.5 kcal mol?1)有所不同。
除了將反式二羥基環(huán)戊烯酮直接用于天然產(chǎn)物合成之外,還證明光水解產(chǎn)物可以應用于更廣泛的合成領域(圖5A)。通過選擇性Wittig反應可以獲得非天然烯烴體系7a。此外,所得醛類化合物可用于還原胺化策略:常見的天然產(chǎn)物吡咯烷酮體系,如內(nèi)酰胺7b,可以通過多米諾式還原胺化-環(huán)化反應獲得(兩步總產(chǎn)率50%)。此外,2-己基呋喃的水解產(chǎn)物4,5-二氧代癸醛3e可以在堿催化下發(fā)生羥醛縮合反應生成烯酮7c(產(chǎn)率52%),該化合物已用于Hedione香料的現(xiàn)代工業(yè)合成。
為了驗證該方法的放大可行性并克服傳統(tǒng)光化學間歇反應中的光衰減效應,作者設計了一種光流反應器(圖 5B)。將藍色 LED 燈帶纏繞在圓柱形玻璃支架上,以全氟烷氧基聚合物管(內(nèi)徑 1.0 mm)作為反應器核心。這種裝置提供了中心對稱且均勻的光照。經(jīng)過工藝優(yōu)化后,2.46 g 的 2-甲基呋喃2a水解生成71%(分離產(chǎn)率為 63%)的4-氧代戊醛 3a,相應的時空產(chǎn)率(STY)為 0.31 kg dm?3 day?1,生產(chǎn)率為 31 mmol day?1。對于呋喃,在流動反應器中產(chǎn)率甚至更高,生成 84% 的丁二醛(3n,蒸餾后分離產(chǎn)率為 46%),相應的STY為 0.78 kg dm?3 day?1,生產(chǎn)率為 90 mmol day?1。此外,通過使用更長的反應管和 30 mL體積的反應器,實現(xiàn)了近三倍的放大,生產(chǎn)率達到 252 mmol day?1,這突顯了本文方法的工藝強化優(yōu)勢。

圖5. 衍生化及應用(圖片來源:Science)
丁二醛具有巨大的應用潛力(圖 5C)。可以將粗呋喃光水解產(chǎn)物濃縮,并通過短程蒸餾獲得純凈的、未聚合的丁二醛(分離產(chǎn)率46%),然后可以將其轉化為 PGF2α 前體 7d。其中一個值得關注的反應是 Tishchenko 環(huán)化反應生成 γ-丁內(nèi)酯,而聚合物工業(yè)對 γ-丁內(nèi)酯的需求量很大。在不進行呋喃光水解產(chǎn)物中間體純化的情況下,使用 [Ru(PPh3)3(CO)HCl]作為催化劑獲得了46%的γ-丁內(nèi)酯產(chǎn)率,這表明該方法具有進一步優(yōu)化的潛力。
總結
聲明:化學加刊發(fā)或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網(wǎng)聯(lián)系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn